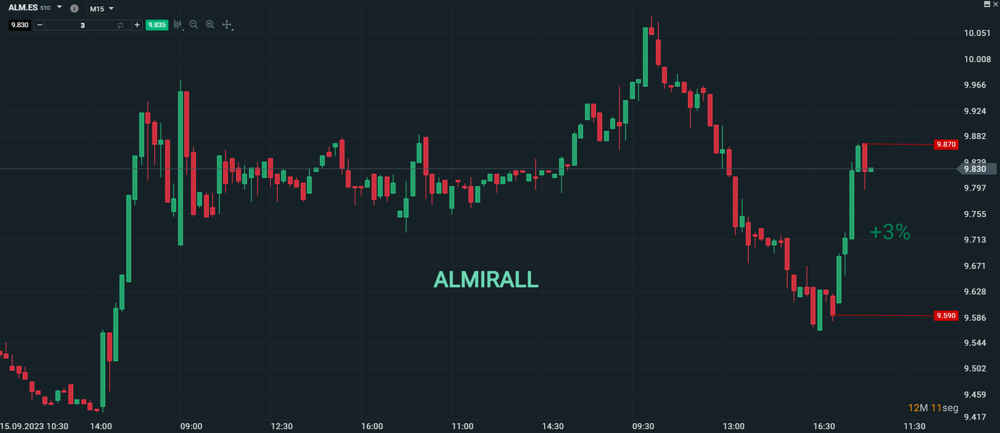
Almirall (ALM.ES) lidera las alzas de la sesión gracia a la aprobación final del Comité de Medicamentos de Uso Humano (Chmp) de la Agencia Europea del Medicamento (EMA) para su medicamento lebrikizumab, destinado al tratamiento de la dermatitis atópica.
Los estudios de fase III han demostrado una respuesta a largo plazo en la mejora de las lesiones cutáneas y el control del picor. Tras esta validación, el medicamento será revisado por la Comisión Europea, con la expectativa de obtener la confirmación de la Unión Europea en aproximadamente dos meses y su lanzamiento en el mercado europeo poco después.
Almirall tiene los derechos exclusivos para comercializar lebrikizumab en Europa, mientras que Eli Lilly and Company tiene los derechos para Estados Unidos y el resto del mundo. Los ensayos clínicos han demostrado que este tratamiento ha ayudado a los pacientes a controlar la enfermedad y mantener los resultados a largo plazo durante 52 semanas, ofreciendo mayor comodidad y flexibilidad en su régimen de dosificación mensual de mantenimiento.
Este medicamento (Lebrikizumab) es un anticuerpo monoclonal en fase de investigación que se dirige a la proteína IL-13, esencial en la dermatitis atópica, al reducir la inflamación de tipo 2 en la piel y aliviar los síntomas como la inflamación, el picor y el engrosamiento de la piel.
Esta noticia es positiva y esperada, ya que se basa en resultados clínicos exitosos. Competirá con Dupixent de Sanofi, por lo que se espera una competencia comercial en el mercado. Como resultado, Almirall ha llegado a subir en la sesión hasta un 3 %.
Análisis realizado por los analistas de XTB